常见有机物分离提纯的几种方法
一、过滤
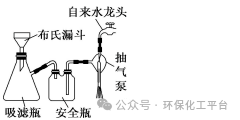
 1、原理:根据固体的溶解度不同,将不溶性固体从溶液中分离出来的方法。2、条件:一种固体不溶,一种固体可溶。3、范围:适用于不溶固体和液体的分离。4、仪器:漏斗、铁架台、烧杯、玻璃棒、滤纸5、注意:一贴二低三靠;对于有些溶液温度下降,会有晶体析出,应该趁热过滤。6、列举:草酸钙中混有醋酸钙:加水溶解,过滤除去醋酸钙溶液。抽滤:又称减压过滤,真空过滤,指利用抽气泵使抽滤瓶中的压强降低,达到固液分离的目的方法。
1、原理:根据固体的溶解度不同,将不溶性固体从溶液中分离出来的方法。2、条件:一种固体不溶,一种固体可溶。3、范围:适用于不溶固体和液体的分离。4、仪器:漏斗、铁架台、烧杯、玻璃棒、滤纸5、注意:一贴二低三靠;对于有些溶液温度下降,会有晶体析出,应该趁热过滤。6、列举:草酸钙中混有醋酸钙:加水溶解,过滤除去醋酸钙溶液。抽滤:又称减压过滤,真空过滤,指利用抽气泵使抽滤瓶中的压强降低,达到固液分离的目的方法。
 二、洗气1、原理:利用气体的溶解性或者化学性质不同,将混合气体分离开来的方法。2、条件:一种气体不溶或不反应,一种气体可溶或可反应。3、范围:适合于混合气体的分离。4、仪器:洗气瓶、导管5、注意:不要引进新的气体杂质,最后能够产生被提纯的气体。6、列举:甲烷中混有乙烯:将混合气体通过溴的四氯化碳溶液,洗去乙烯。三、蒸发
二、洗气1、原理:利用气体的溶解性或者化学性质不同,将混合气体分离开来的方法。2、条件:一种气体不溶或不反应,一种气体可溶或可反应。3、范围:适合于混合气体的分离。4、仪器:洗气瓶、导管5、注意:不要引进新的气体杂质,最后能够产生被提纯的气体。6、列举:甲烷中混有乙烯:将混合气体通过溴的四氯化碳溶液,洗去乙烯。三、蒸发
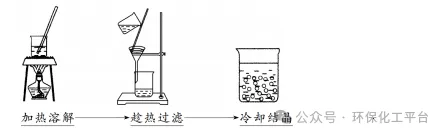
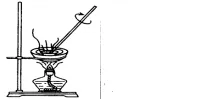 1、原理:把可溶性固体从溶剂中分离出来的方法。2、条件:固体可溶3、范围:适合于把可溶性固体从溶剂中分离出来。4、仪器:铁架台、蒸发皿、酒精灯、玻璃棒5、注意:玻璃棒作用;溶剂易挥发或易燃烧,采用水浴加热。6、列举:从醋酸钠溶液中提取醋酸钠:蒸发溶液,使醋酸钠析出。四、结晶1、原理:通过蒸发溶剂或者降低温度使溶质的溶解度变小,从而使晶体析出的方法。2、条件:固体的溶解度小或者固体的溶解度随温度升高变化较大。3、范围:固体的溶解度小一般用蒸发结晶法;固体的溶解度随温度升高变化较大,一般用冷却结晶法或者重结晶法。4、仪器:过滤、蒸发仪器。5、注意:基本环节:溶解—蒸发浓缩—趁热过滤—冷却结晶—洗涤干燥6、列举:苯甲酸钠中混有氯化钠:加水溶解,蒸发浓缩,冷却结晶,就可以除去氯化钠。结晶的方法:①蒸发结晶;②降温结晶(蒸发浓缩、冷却结晶)蒸发结晶:蒸发溶剂,使溶液由不饱和变为饱和,继续蒸发,过剩的溶质就会呈晶体析出降温结晶:先加热溶液,蒸发溶剂成饱和溶液,此时降低热饱和溶液的温度,溶解度随温度变化较大的溶质就会呈晶体析出。结晶方法的选择:Ⅰ、当溶液为单一溶质时:①晶体不带结晶水,如NaCl、KNO3等:蒸发结晶;②晶体带结晶水,如胆矾等:将滤液蒸发浓缩、冷却结晶、过滤。Ⅱ、当溶液为两种以上溶质时:①得到溶解度受温度影响小的溶质:蒸发浓缩结晶,趁热过滤 (如除去NaCl中少量的KNO3);②得到溶解度受温度影响大的溶质:蒸发浓缩、冷却结晶,过滤(如除去KNO3中少量的NaCl)。重结晶:是将晶体溶于溶剂以后,又重新从溶液结晶的过程。重结晶可以使不纯净的物质获得纯化,或使混合在一起的盐类彼此分离。过程:1.将需要纯化的化学试剂溶解于沸腾或将进沸腾的适宜溶剂中; 2.将热溶液趁热过滤,以除去不溶的杂质; 3.将滤液冷却,使结晶析出; 4.滤出结晶,必要时用适宜的溶剂洗涤结晶(1)适用条件①重结晶是提纯固态有机物的常用方法。②杂质在所选溶剂中溶解度很小或很大,易于除去。③被提纯的有机物在所选溶剂中的溶解度,受温度的影响较大;该有机物在热溶液中的溶解度较大,在冷溶液中的溶解度较小,冷却后易于结晶析出。(2)实验仪器与操作步骤
1、原理:把可溶性固体从溶剂中分离出来的方法。2、条件:固体可溶3、范围:适合于把可溶性固体从溶剂中分离出来。4、仪器:铁架台、蒸发皿、酒精灯、玻璃棒5、注意:玻璃棒作用;溶剂易挥发或易燃烧,采用水浴加热。6、列举:从醋酸钠溶液中提取醋酸钠:蒸发溶液,使醋酸钠析出。四、结晶1、原理:通过蒸发溶剂或者降低温度使溶质的溶解度变小,从而使晶体析出的方法。2、条件:固体的溶解度小或者固体的溶解度随温度升高变化较大。3、范围:固体的溶解度小一般用蒸发结晶法;固体的溶解度随温度升高变化较大,一般用冷却结晶法或者重结晶法。4、仪器:过滤、蒸发仪器。5、注意:基本环节:溶解—蒸发浓缩—趁热过滤—冷却结晶—洗涤干燥6、列举:苯甲酸钠中混有氯化钠:加水溶解,蒸发浓缩,冷却结晶,就可以除去氯化钠。结晶的方法:①蒸发结晶;②降温结晶(蒸发浓缩、冷却结晶)蒸发结晶:蒸发溶剂,使溶液由不饱和变为饱和,继续蒸发,过剩的溶质就会呈晶体析出降温结晶:先加热溶液,蒸发溶剂成饱和溶液,此时降低热饱和溶液的温度,溶解度随温度变化较大的溶质就会呈晶体析出。结晶方法的选择:Ⅰ、当溶液为单一溶质时:①晶体不带结晶水,如NaCl、KNO3等:蒸发结晶;②晶体带结晶水,如胆矾等:将滤液蒸发浓缩、冷却结晶、过滤。Ⅱ、当溶液为两种以上溶质时:①得到溶解度受温度影响小的溶质:蒸发浓缩结晶,趁热过滤 (如除去NaCl中少量的KNO3);②得到溶解度受温度影响大的溶质:蒸发浓缩、冷却结晶,过滤(如除去KNO3中少量的NaCl)。重结晶:是将晶体溶于溶剂以后,又重新从溶液结晶的过程。重结晶可以使不纯净的物质获得纯化,或使混合在一起的盐类彼此分离。过程:1.将需要纯化的化学试剂溶解于沸腾或将进沸腾的适宜溶剂中; 2.将热溶液趁热过滤,以除去不溶的杂质; 3.将滤液冷却,使结晶析出; 4.滤出结晶,必要时用适宜的溶剂洗涤结晶(1)适用条件①重结晶是提纯固态有机物的常用方法。②杂质在所选溶剂中溶解度很小或很大,易于除去。③被提纯的有机物在所选溶剂中的溶解度,受温度的影响较大;该有机物在热溶液中的溶解度较大,在冷溶液中的溶解度较小,冷却后易于结晶析出。(2)实验仪器与操作步骤
 五、分液1、原理:把互不相溶的液体分离开来的方法。2、条件:液体互不相溶3、范围:适合于互不相溶的液体分离。4、仪器:分液漏斗、烧杯5、注意:分液漏斗的基本操作6、列举:己烷中混有己烯:加入酸性高锰酸钾溶液,振荡后用分液漏斗分离。六、萃取
五、分液1、原理:把互不相溶的液体分离开来的方法。2、条件:液体互不相溶3、范围:适合于互不相溶的液体分离。4、仪器:分液漏斗、烧杯5、注意:分液漏斗的基本操作6、列举:己烷中混有己烯:加入酸性高锰酸钾溶液,振荡后用分液漏斗分离。六、萃取
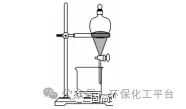 (1)萃取原理①液—液萃取:利用有机物在两种互不相溶的溶剂中的溶解性不同,将有机物从一种溶剂转移到另一种溶剂的过程。②固—液萃取:用有机溶剂从固体物质中溶解出有机物的过程。(2)仪器:分液漏斗、烧杯、铁架台。(3)操作要求:加萃取剂后充分振荡,静置分层后,打开分液漏斗活塞,从下口将下层液体放出,并及时关闭活塞,上层液体从上口倒出。(4)萃取剂选用原则:1.萃取剂和原溶剂互不混溶。2.萃取剂和溶质互不发生反应。3.溶质在萃取剂中的溶解度远大于在原溶剂中的溶解度 (5)反萃取:是用反萃取剂使被萃取物从负载有机相返回水相的过程,为萃取的逆过程。反萃取可将有机相中各个被萃组分逐个反萃到水相,使被分离组分得到分离;也可一次将有机相中被萃组分反萃到水相。经过反萃取及所得反萃液经过进一步处理后,便得到被分离物的成品。反萃后经洗涤不含或少含萃合物的有机相称再生有机相,继续循环使用。七、蒸馏
(1)萃取原理①液—液萃取:利用有机物在两种互不相溶的溶剂中的溶解性不同,将有机物从一种溶剂转移到另一种溶剂的过程。②固—液萃取:用有机溶剂从固体物质中溶解出有机物的过程。(2)仪器:分液漏斗、烧杯、铁架台。(3)操作要求:加萃取剂后充分振荡,静置分层后,打开分液漏斗活塞,从下口将下层液体放出,并及时关闭活塞,上层液体从上口倒出。(4)萃取剂选用原则:1.萃取剂和原溶剂互不混溶。2.萃取剂和溶质互不发生反应。3.溶质在萃取剂中的溶解度远大于在原溶剂中的溶解度 (5)反萃取:是用反萃取剂使被萃取物从负载有机相返回水相的过程,为萃取的逆过程。反萃取可将有机相中各个被萃组分逐个反萃到水相,使被分离组分得到分离;也可一次将有机相中被萃组分反萃到水相。经过反萃取及所得反萃液经过进一步处理后,便得到被分离物的成品。反萃后经洗涤不含或少含萃合物的有机相称再生有机相,继续循环使用。七、蒸馏
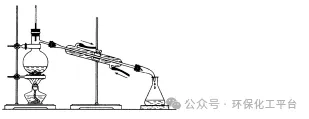 1、原理:利用液体的沸点不同,经过加热冷凝使液体分离的操作。2、条件:液体的沸点相差比较大。3、范围:适合于沸点不同的液体的分离。4、仪器:酒精灯、铁架台、石棉网、蒸馏烧瓶、冷凝管、接应管、锥形瓶、温度计5、注意:温度计位置;逆流冷凝。6、列举:酒精中混有水,加氧化钙,蒸馏可除去水。
1、原理:利用液体的沸点不同,经过加热冷凝使液体分离的操作。2、条件:液体的沸点相差比较大。3、范围:适合于沸点不同的液体的分离。4、仪器:酒精灯、铁架台、石棉网、蒸馏烧瓶、冷凝管、接应管、锥形瓶、温度计5、注意:温度计位置;逆流冷凝。6、列举:酒精中混有水,加氧化钙,蒸馏可除去水。
 电渗析高性价比的物料浓缩/分离/再生新秀——电渗析技术八、渗析1、原理:利用半透膜能够透过离子或分子,不能透过胶粒的性质分离提纯胶体的操作。2、条件:一种是胶体,一种是溶液3、范围:适合分离胶体和溶液。4、仪器:烧杯、半透膜袋5、注意:最好在流动的水中进行6、列举:鸡蛋白中混有少量氯化钠:把混合溶液装在半透膜袋中,置于流动的水中。九、盐析1、原理:利用轻金属盐能够降低胶体的溶解度的性质,分离提纯胶体的方法。2、条件:一种是胶体,一种是溶剂3、范围:适合胶体和溶剂的分离4、仪器:烧杯、过滤装置5、注意:方法是盐析,操作是过滤6、列举:硬脂酸钠中混有甘油:加少量食盐,使硬脂酸钠析出,然后过滤分离。十、色谱
电渗析高性价比的物料浓缩/分离/再生新秀——电渗析技术八、渗析1、原理:利用半透膜能够透过离子或分子,不能透过胶粒的性质分离提纯胶体的操作。2、条件:一种是胶体,一种是溶液3、范围:适合分离胶体和溶液。4、仪器:烧杯、半透膜袋5、注意:最好在流动的水中进行6、列举:鸡蛋白中混有少量氯化钠:把混合溶液装在半透膜袋中,置于流动的水中。九、盐析1、原理:利用轻金属盐能够降低胶体的溶解度的性质,分离提纯胶体的方法。2、条件:一种是胶体,一种是溶剂3、范围:适合胶体和溶剂的分离4、仪器:烧杯、过滤装置5、注意:方法是盐析,操作是过滤6、列举:硬脂酸钠中混有甘油:加少量食盐,使硬脂酸钠析出,然后过滤分离。十、色谱
 1、原理:利用吸附剂对不同有机物的吸附作用不同分离提纯有机物的操作。2、条件:同一吸附剂吸附有机物能力不同。3、范围:适合分离吸附能力不同的有机物。4、仪器:吸附柱5、注意:选择碳酸钙、硅胶、氧化铝、活性炭等吸附剂6、列举:叶绿素和叶黄素的分离:以碳酸钙粉末为吸附剂,装入吸附柱中,加入混合物分离。【鉴别】常见有机物的鉴别主要根据有机物分子结构中所含官能团不同,常用试剂产生的现象官能团确定常见有机物类别金属钠产生气体(H2)含—OH醇、酚、羧酸NaHCO3产生气体(CO2)羧酸KMnO4(H+)溶液褪色不饱和键、有侧链的苯环、羟基、醛基烯、炔、苯的同系物、醇、酚、醛、醛糖溴水褪色、产生白色沉淀不饱和键、醛基、酚羟基烯、炔、醛、醛糖、酚萃取分层—X烷烃、芳烃、卤代烃银氨溶液热水浴,产生银镜醛、甲酸、甲酸酯、葡萄糖新制Cu(OH)2常温,蓝色沉淀溶解加热产生红色沉淀 低级羧酸、 醛、甲酸、甲酸酯、葡萄糖FeCl3溶液溶液变紫色酚羟基说明:A.醇、酚、羧酸的鉴别能用其它方法时不能用金属钠。B.不同有机物的鉴别有时也可利其水溶性和密度(如烃、酯比水轻,而溴代烃、四氯化碳、硝基苯比水重)。 【分离和除杂质】有机物的分离或除杂质一般根据各有机物的化学性质、常温状态、溶解性、沸点的不同,常采用洗气、分液或蒸馏的方法。a.固—固混合分离型:灼烧、升华、热分解、结晶(重结晶)等。b.固—液混合分离型:过滤、盐析、蒸发结晶、冷却结晶(重结晶)等。c.液—液混合分离型:萃取、分液、蒸馏等。d.气—气混合分离型:洗气(采用液体净化剂时用洗气瓶,采用固体净化剂时用干燥管)。在一个具体的分离和提纯过程中,往往同时用到几种不同的方法,同时还要使用化学方法。其基本原则是:(1)尽可能使加入的试剂只跟杂质发生作用;(2)提纯物质过程不能引入新的杂质;(3)杂质与试剂反应生成的产物易分离出来;(4)提纯过程应做到方法简单、现象明显、分离容易、所得产物纯度高;(5)尽可能将杂质转化为原料;(6)若要求“分离”则必须恢复被提纯物质原来的组成和状态:即“不增、不减、易分、复原”四原则。(1).分离:常见不同状态的有机混合物的分离方法如下表:有机混合物分离方法使用主要仪器气体混合物洗气洗气瓶不相溶的液体混合物分液分液漏斗相溶液体(沸点差距大)蒸馏蒸馏烧瓶(2).除杂质常见有机化合物中含有的杂质、除杂试剂和方法如下表:(括号内物质为杂质)有机混合物常用除杂试剂方法①CH4(C2H4)溴水洗气②CH3CH2Br(乙醇)水 分液③CH3CH2OH(H2O)新制生石灰蒸馏④乙酸乙酯(乙酸)饱和Na2CO3溶液分液⑤苯(甲苯)高锰酸钾溶液、氢氧化钠溶液蒸馏⑥.溴苯(溴)氢氧化钠溶液分液⑦苯(苯酚)氢氧化钠溶液分液⑧.硝基苯(硝酸、硫酸)氢氧化钠溶液分液
1、原理:利用吸附剂对不同有机物的吸附作用不同分离提纯有机物的操作。2、条件:同一吸附剂吸附有机物能力不同。3、范围:适合分离吸附能力不同的有机物。4、仪器:吸附柱5、注意:选择碳酸钙、硅胶、氧化铝、活性炭等吸附剂6、列举:叶绿素和叶黄素的分离:以碳酸钙粉末为吸附剂,装入吸附柱中,加入混合物分离。【鉴别】常见有机物的鉴别主要根据有机物分子结构中所含官能团不同,常用试剂产生的现象官能团确定常见有机物类别金属钠产生气体(H2)含—OH醇、酚、羧酸NaHCO3产生气体(CO2)羧酸KMnO4(H+)溶液褪色不饱和键、有侧链的苯环、羟基、醛基烯、炔、苯的同系物、醇、酚、醛、醛糖溴水褪色、产生白色沉淀不饱和键、醛基、酚羟基烯、炔、醛、醛糖、酚萃取分层—X烷烃、芳烃、卤代烃银氨溶液热水浴,产生银镜醛、甲酸、甲酸酯、葡萄糖新制Cu(OH)2常温,蓝色沉淀溶解加热产生红色沉淀 低级羧酸、 醛、甲酸、甲酸酯、葡萄糖FeCl3溶液溶液变紫色酚羟基说明:A.醇、酚、羧酸的鉴别能用其它方法时不能用金属钠。B.不同有机物的鉴别有时也可利其水溶性和密度(如烃、酯比水轻,而溴代烃、四氯化碳、硝基苯比水重)。 【分离和除杂质】有机物的分离或除杂质一般根据各有机物的化学性质、常温状态、溶解性、沸点的不同,常采用洗气、分液或蒸馏的方法。a.固—固混合分离型:灼烧、升华、热分解、结晶(重结晶)等。b.固—液混合分离型:过滤、盐析、蒸发结晶、冷却结晶(重结晶)等。c.液—液混合分离型:萃取、分液、蒸馏等。d.气—气混合分离型:洗气(采用液体净化剂时用洗气瓶,采用固体净化剂时用干燥管)。在一个具体的分离和提纯过程中,往往同时用到几种不同的方法,同时还要使用化学方法。其基本原则是:(1)尽可能使加入的试剂只跟杂质发生作用;(2)提纯物质过程不能引入新的杂质;(3)杂质与试剂反应生成的产物易分离出来;(4)提纯过程应做到方法简单、现象明显、分离容易、所得产物纯度高;(5)尽可能将杂质转化为原料;(6)若要求“分离”则必须恢复被提纯物质原来的组成和状态:即“不增、不减、易分、复原”四原则。(1).分离:常见不同状态的有机混合物的分离方法如下表:有机混合物分离方法使用主要仪器气体混合物洗气洗气瓶不相溶的液体混合物分液分液漏斗相溶液体(沸点差距大)蒸馏蒸馏烧瓶(2).除杂质常见有机化合物中含有的杂质、除杂试剂和方法如下表:(括号内物质为杂质)有机混合物常用除杂试剂方法①CH4(C2H4)溴水洗气②CH3CH2Br(乙醇)水 分液③CH3CH2OH(H2O)新制生石灰蒸馏④乙酸乙酯(乙酸)饱和Na2CO3溶液分液⑤苯(甲苯)高锰酸钾溶液、氢氧化钠溶液蒸馏⑥.溴苯(溴)氢氧化钠溶液分液⑦苯(苯酚)氢氧化钠溶液分液⑧.硝基苯(硝酸、硫酸)氢氧化钠溶液分液